病原体核酸质控物使用及注意事项
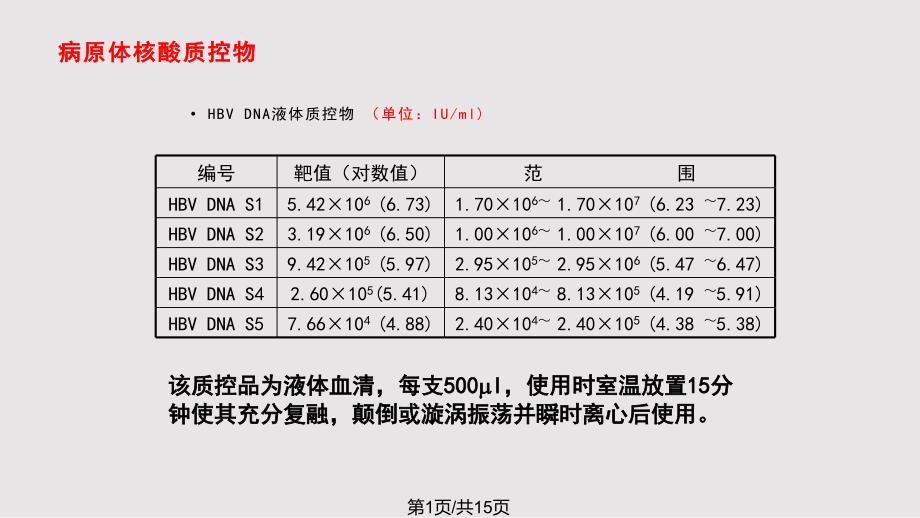
病原体核酸质控物病原体核酸质控物HBV DNA液体质控物(单位:IU/ml)编号靶值(对数值)范 围HBV DNA S15.42106(6.73)1.70106 1.70107(6.23 7.23)HBV DNA S23.19106(6.50)1.00106 1.00107(6.00 7.00)HBV DNA S39.42105(5.97)2.95105 2.95106(5.47 6.47)HBV DNA S42.60105(5.41)8.13104 8.13105(4.19 5.91)HBV DNA S57.66104(4.88)2.40104 2.40105(4.38 5.38)该质控品为液体血清,每支该质控品为液体血清,每支500500 l l,使用时室温放置,使用时室温放置1515分分钟使其充分复融,颠倒或漩涡振荡并瞬时离心后使用钟使其充分复融,颠倒或漩涡振荡并瞬时离心后使用第1页/共15页HCV RNAHCV RNA冻干质控物冻干质控物 (单位:(单位:IU/ml)IU/ml)病原体核酸质控物病原体核酸质控物编号靶值(对数值)范 围07111.32106(6.12)4.17105 1.70106(5.626.62)07121.05106(6.02)3.31105 3.31106(5.526.52)07135.76105(5.76)1.82105 1.82106(5.266.26)07156.61103(3.82)2.09103 2.09104(3.324.32)07168.72104(4.94)2.75104 2.75105(4.445.44)该质控品为冻干血清,每支该质控品为冻干血清,每支300300 l l,使用时用,使用时用DEPCDEPC水复溶,水复溶,室温放置室温放置5 5分钟,漩涡振荡使之充分溶解并混匀,瞬时离心分钟,漩涡振荡使之充分溶解并混匀,瞬时离心后使用。
后使用第2页/共15页病原体核酸质控物病原体核酸质控物 关于定量单位IU/ml和拷贝数/ml的换算请根据不同试剂的检测结果与该质控品的定值进行比对得出,不同试剂的换算系数会有所不同IU/ml拷贝数/mlWHO各不同试剂厂家病毒个数“检出单位”(detectable unit)假设:PCR反应体系内含有1 拷贝的待测分子即可检出 第3页/共15页拷贝数拷贝数/ml/ml的确定:的确定:DNA/RNA 参考品(质粒等)参考品(质粒等)测量OD260的值得到mg/ml通过与分子量的计算,得到拷贝数/ml不同实验室得到的结果差别很大第4页/共15页HCVHCV国际单位与拷贝数换算国际单位与拷贝数换算NGI NGI SuperQuant:SuperQuant:1 IU/mL=3.4 copies/ml1 IU/mL=3.4 copies/ml (NGI Product License Application to FDA)(NGI Product License Application to FDA)Roche Roche AmplicorAmplicor 1 1 IU/mL=IU/mL=0.9 copies/ml0.9 copies/ml (Roche Molecular Systems)(Roche Molecular Systems)Cobas AmplicorCobas Amplicor 1 IU/mL=2.7 copies/ml1 IU/mL=2.7 copies/ml (Roche Molecular Systems)(Roche Molecular Systems)LCx HCV RNA Quantitative AssayLCx HCV RNA Quantitative Assay 1 IU/mL=3.8 copies/ml1 IU/mL=3.8 copies/ml (Abbott Diagnostics)(Abbott Diagnostics)Bayer bDNA 3.0:Bayer bDNA 3.0:1 IU/mL=5.2 copies/ml1 IU/mL=5.2 copies/ml (Bayer Development Group)(Bayer Development Group)第5页/共15页未知未知HCV RNA 样本样本甲实验室 5000拷贝/ml 乙实验室 10000拷贝/ml 丙实验室 50000拷贝/ml 丁实验室 20000拷贝/ml 实验室结果的互通性实验室结果的互通性第6页/共15页20000IU/mlHCV RNA 样本样本甲实验室 40000拷贝/ml1IU/ml2拷贝/ml 乙实验室 10000拷贝/ml 1IU/ml拷贝/ml丙实验室 50000拷贝/ml1IU/ml拷贝/ml 丁实验室 20000拷贝/ml1IU/ml1拷贝/ml 实验室结果的互通性实验室结果的互通性第7页/共15页国家标准物质国家标准物质在国际上,发达国家的试剂厂家均采用可溯源到国际标准的标准系列来进行定量检测,而我国的试剂生产厂家标准来源、定量单位均不统一,造成检测结果存在10倍乃至100倍的差异。
卫生部临床检验中心参考世界卫生组织(WHO)相关项目标准物质的研制方法,研制了HBV DNA和HCV RNA标准物质1)将该标准物质用于各试剂厂家定标;(2)依据该标准品制备标准系列血清用作厂家试剂的工作标准;(3)向全国提供可溯源到该标准物质的室内质控品第8页/共15页IUIU(international units)international units)的确定:的确定:22家实验室实验1实验2实验3实验4间隔1周7次10倍稀释8次101/2倍稀释(终点浓度附近)“终点”Report on the evaluation of a candidate standard for NAT assays for HCV RNA第9页/共15页1:101:1001:316 1:1000 1:3160HCV RNA 终点稀释终点稀释:1:100001 12 23 34 45 56 67 78 89 910101111Poisson分布:63的实验室检测结果为阳性的稀释倍数定为“终点”,即1IU/mlIUIU(international units)international units)的确定:的确定:第10页/共15页核酸质控物的定值核酸质控物的定值实验室数方法均值3Amplicor Monitor3bDNA2In-house1NASBA6改良的Amplicor(定性)9单一PCR(定性)6巢式PCR(定性)统计学计算得出均值定值的标准品核酸质控物第11页/共15页该质控品是具有生物活性的样品并具有传染性,请使用务必按传染性样品对待。
实验室收到血清后应将血清保存在18以下,保质期为1年定性测定:一份弱阳性(接近测定下限)和一份阴性质控(依样本数量而定)定量测定:高、中、低三种浓度的质控样本使用注意事项使用注意事项第12页/共15页使用注意事项定量测定要根据试验的测定范围,采用高中低三种浓度的质控样本第13页/共15页谢 谢!第14页/共15页感谢您的观看!第15页/共15页。




